รพ.จุฬาลงกรณ์ ปั้นวัคซีน ‘ChulaCov19’ เทคโนโลยี mRNA สัญชาติไทย เผยผลทดลองในมนุษย์ระยะที่ 1 ได้ผลดีประสิทธิผลเทียบเคียงไฟเซอร์ เร่งเดินหน้าเฟส 2 ตั้งเป้าสูงสุดผลิตออกมาทัน เม.ย. 65 เล็งใช้เป็นเข็ม 3 พร้อมต่อยอดสร้างสูตร 2-3 รับไวรัสกลายพันธุ์
วันที่ 16 สิงหาคม 2564 ปัจจุบันสภาวการณ์การแพร่ระบาดของโควิดในไทยทวีความรุนแรงต่อเนื่อง จากโควิดระลอก 3 ที่ขณะนี้มีสายพันธุ์เดลต้าเป็นตัวหลัก ผลักยอดผู้ป่วยทะลุ 20,000 ราย/วัน และมีแนวโน้มเพิ่มสูงขึ้นแม้มีการนำมาตรการล็อกดาวน์บางส่วนมาใช้แล้วก็ตาม ขณะที่การพึ่งพิงการนำเข้าวัคซีนจากต่างประเทศเพียงอย่างเดียวอาจไม่เพียงพอต่อสถานการณ์ฉุกเฉินเช่นนี้ ดังนั้น การผลิตวัคซีนโควิดเพื่อใช้เองภายในประเทศอาจดูจะเหมาะสมที่สุดสำหรับประเทศไทยในระยะยาว
- ลูกแม่ค้าขายผัก-พ่อขับแท็กซี่ สู่เก้าอี้ “ปลัดพลังงาน” บทพิสูจน์ชีวิต “ดร.ประเสริฐ สินสุขประเสริฐ”
- NETA X ขาย มิ.ย.นี้ ราคาไม่เกิน 1 ล้านบาท หลัง MOU สรรพสามิต
- KBANK ปรับโครงสร้างใหญ่ ลดจำนวนบอร์ด ตั้ง 4 เอ็มดีเป็น “ผู้จัดการใหญ่” มีผล 1 พ.ค.67
ศ.นพ.เกียรติ รักษ์รุ่งธรรม ผู้อำนวยการบริหารโครงการพัฒนาวัคซีนโควิด-19 ศูนย์วิจัยวัคซีน คณะแพทยศาสตร์ จุฬาลงกรณ์มหาวิทยาลัย และโรงพยาบาลจุฬาลงกรณ์ สภากาชาดไทย เปิดเผยว่า การพัฒนาวัคซีนป้องกันโควิด 19 เทคโนโลยี mRNA ภายใต้ชื่อ “ChulaCov19” หรือจุฬาคอฟ 19 ปัจจุบันได้ผ่านการทดลองในมนุษย์เฟสที่ 1 ไปได้ระยะหนึ่งแล้ว สำหรับกลุ่มอายุ 18-55 ปี จำนวน 36 คน ขณะที่อาสาสมัครกลุ่มสูงวัยอายุ 56-75 ปี ยังอยู่ระหว่างการฉีดเข็มที่ 2
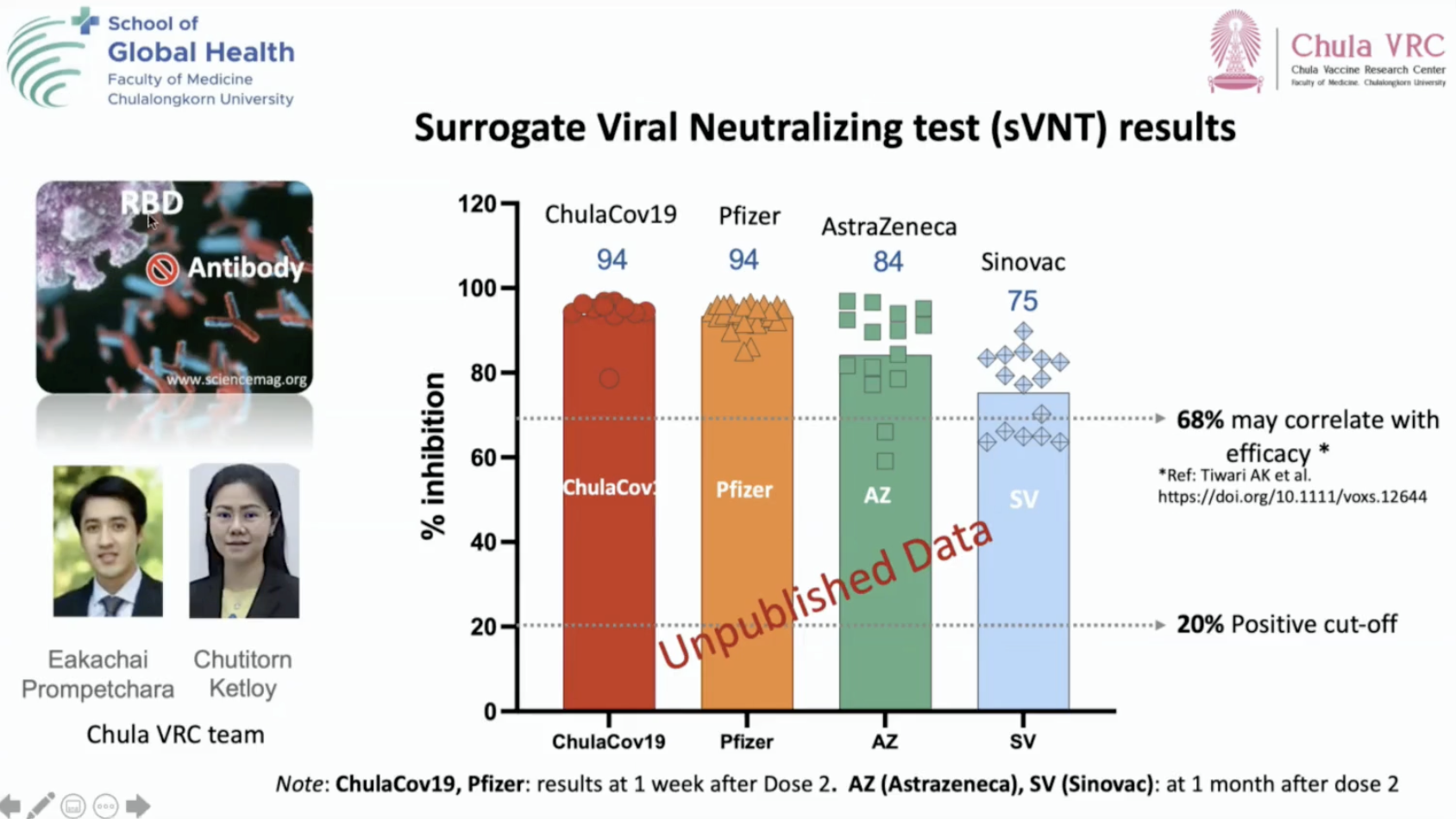
ทั้งนี้ ผลจากการทดลองดังกล่าวในกลุ่มอายุ 18-55 ปี พบว่ามีอัตราการยับยั้งการติดเชื้อสูงเทียบเท่าไฟเซอร์ที่ 94% ขณะที่แอสตร้าเซนเนก้าและซิโนแวคมีประสิทธิภาพยับยั้ง 84% และ 68% ตามลำดับ
หากแยกตามสายพันธุ์พบว่ามีค่าป้องกันเชื้อดั้งเดิมได้ที่ 1,258 ส่วนอัลฟ่า (อังกฤษ) อยู่ที่ 968 และเดลต้า (อินเดีย) 977 ถือว่ามีค่าลดลงเล็กน้อย สวนทางกับสายพันธุ์เบต้าและแกมม่าที่มีค่าลดลงสูงเหลือเพียง 343 และ 372 ตามลำดับ ส่วนอาการข้างเคียงหลังฉีดวัคซีนมีเล็กน้อย อยู่ในระดับไม่รุนแรง เช่น เป็นไข้ หนาวสั่น ปวดบริเวณที่ฉีด
และหากเจาะลึกลงไปในระดับทีเซลล์ (T-Cell) ซึ่งจะสามารถขจัดและควบคุมเชื้อที่อยู่ในเซลล์ของผู้ป่วยที่ติดเชื้อโควิดได้ แต่ต้องย้ำว่าการทดสอบนี้ยังจำนวนไม่มาก ซึ่งยังเป็นผลเบื้องต้น
“วัคซีน ChulaCov19 สำหรับผลการทดลองเฟสที่ 1 ในมนุษย์ถือว่าได้ผลตอบรับดี สามารถยับยั้งได้ทั้ง 4 สายพันธุ์ โดยเบื้องต้นเป้าหมายสูงสุดของเราคือการผลิตเพื่อใช้กับคนไทยให้ทันภายในเมษายน 2565 ซึ่งคาดว่าในช่วงดังกล่าวคนไทยมากกว่า 80% น่าจะฉีดวัคซีนป้องกันโควิดครอบคลุมแล้ว จึงตั้งใจให้วัคซีนตัวดังกล่าวสามารถเป็นเข็มที่ 3 สำหรับบูสเตอร์โดสได้ ส่วนระยะต่อไปจะเริ่มทดลองในเฟส 2A และ 2B เพื่อให้ได้ผลการทดลองกับมนุษย์ในวงกว้างมากขึ้น คาดว่าจะใช้เงินลงทุนราว 500-600 ล้านบาท”
อย่างไรก็ดี ถ้าตามกติกาสากลทั่วไปการทดลองในมุษย์ต้องมีถึงเฟส 3 ดังนั้น ถ้าเป็นเช่นนี้ในเดือนเมษายน 2565 ก็อาจจะไม่ทัน
ในส่วนโรงงานที่จะผลิตอยู่ที่ จ.พระนครศรีอยุธยา เป็นของ BionetAsia ซึ่งหากเป็นไปตามแผนจะมีวัคซีนที่ผลิตโดยคนไทยและในประเทศไทยภายในเดือนตุลาคม ปี 2565
พร้อมกันนี้ เพื่อป้องกันโควิดสายพันธุ์เดลต้า แกมม่า และเบต้า ให้ดียิ่งขึ้น ได้พัฒนาวัคซีนรับการกลายพันธุ์ในรุ่นที่ 2 และ 3 ขนานกันไปอีกด้วย
ศ.นพ.เกียรติ กล่าวต่อไปว่า สิ่งที่อยากฝากไว้คือ ถ้าประเทศไทยต้องการให้มีอย่างน้อย 1 ใน 4 วัคซีนได้รับการรับรองให้เป็นวัคซีนในภาวะฉุกเฉิน EUA by April 2002 ต้องทำอย่างไรนั้น เบื้องต้นต้องมี 4 องค์ประกอบ ได้แก่
1.การระดมทุน ต้องมีเป้าหมายร่วมกันทั้งรัฐและเอกชน และประชาชนต้องมีงบเพียงพอ
2.กติกาในการขึ้นทะเบียนวัคซีน ต้องมีกติกาออกมาชัดเจนภายในเดือนหน้า จาก อย. ว่าการขึ้นทะเบียนจะต้องทำวิจัยระยะสองบี และหรือระยะสามอย่างไร จึงจะเพียงพอ
3.โรงงานผลิต ต้องเร่งดำเนินการให้สามารถรผลิตวัคซีนที่มีคุณภาพและจำนวนมากได้ก่อนสิ้นปี
4.นโยบายการจองและจัดซื้อวัคซีนล่วงหน้าต้องมีความชัดเจน